Contents
Muse細胞は何が新しいのか
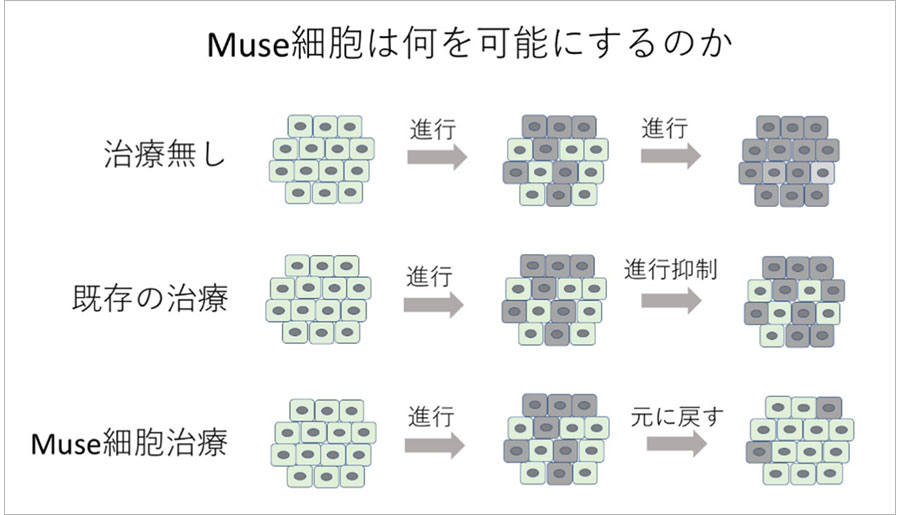
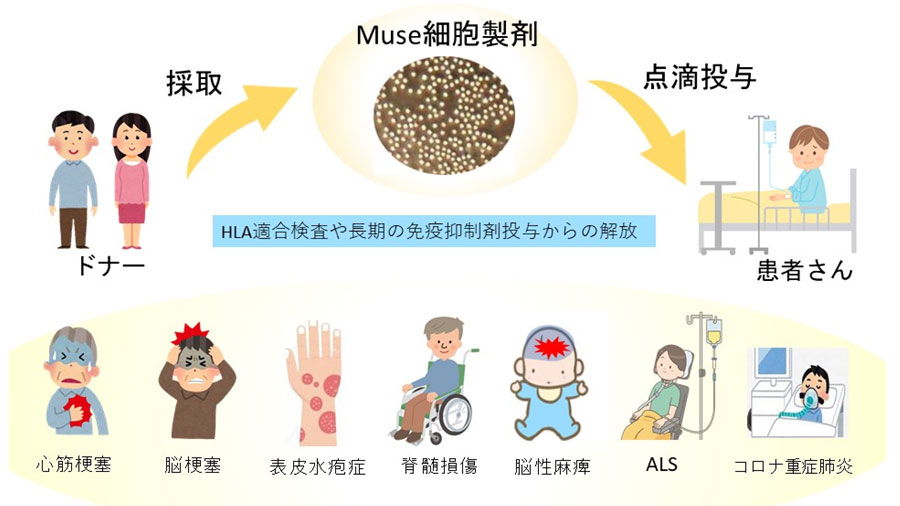
Muse細胞は何を可能にするのか
臓器は細胞という機能的な単位が集合したものです。何らかの理由で細胞が傷害されたり死んで脱落しますと組織は変性し、臓器としての機能を果たせなくなります。現在、既存の治療法では傷ついて失われた細胞を元に戻す有効な方法はありません。Muse細胞は、傷害を受けた臓器に集積し、傷ついたり死んだ細胞と同じ種類の細胞に自ら分化することで細胞を置換し、組織を修復します。これがMuse細胞治療の特徴となります。
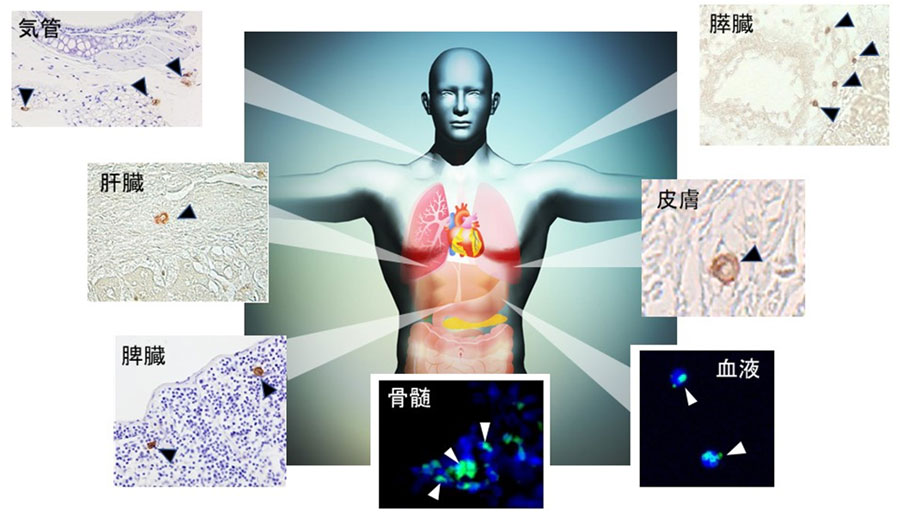
Muse細胞は我々の体内にある自然の幹細胞
多能性幹細胞の代表的な細胞表面マーカー Stage-specific embryonic antigen-3 (SSEA-3)で標識・同定することが可能です。骨髄、末梢血、各臓器に散在性に存在します(図の白あるいは黒の矢頭はSSEA-3陽性のMuse細胞)。また臍帯など胎児付属組織にも存在します。骨髄では有核細胞の約3000分の1(0.03%)の割合で存在します。末梢血はかなり個人差がありますが有核細胞の約3000分の1(0.03%)から約1000分の1(0.1%)の割合で存在しますが、疾患があると大きく変動します。
生体の中に自然に存在するため、腫瘍化のような安全性の懸念が低いことが分かっております。腫瘍化の一つの指標であるテロメラーゼ活性を調べますと、腫瘍性を有する細胞よりも低く、線維芽細胞などの通常の体細胞と同等のレベルを示します。生体に移植後半年経過しても腫瘍が形成されないことも、動物実験で確認されています。
多能性幹細胞としてのMuse細胞
我々の体は発生学的に内胚葉、外胚葉、中胚葉いずれかに由来する細胞から構成されております。多能性であるということは、これら3胚葉性のいずれの細胞にも分化できる能力をもつことを意味します。Muse細胞は神経細胞、色素細胞、角化細胞などの外胚葉性、胆管細胞、肝細胞、β細胞などの内胚葉性、腎臓糸球体細胞、血管内皮、心筋、脂肪細胞、骨細胞などの中胚葉性の細胞に分化することが分かっております。
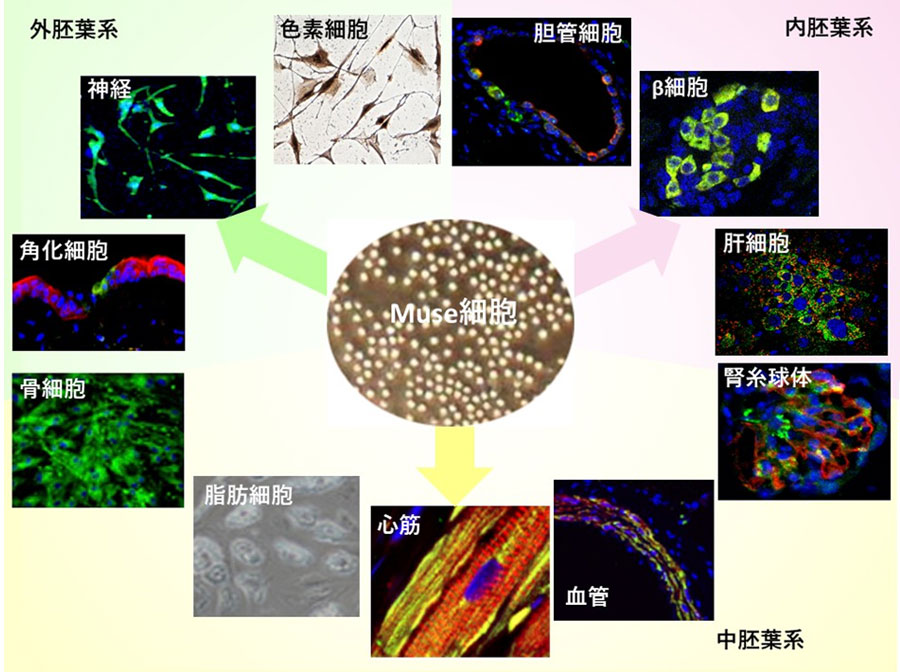
さらに3胚葉性に分化できる娘細胞が細胞分裂によって作られ維持されることから、自己複製能があると考えられております。このことから、Muse細胞は多能性幹細胞であると考えられます。
修復幹細胞としての働き
Muse細胞は一定の割合で骨髄から末梢血に動員され、血液中を巡りながら様々な臓器に分配されていると考えられています。我々の臓器はミクロレベルで日々傷害を受けたり、細胞が死んで脱落しております。Muse細胞は多能性ですので、各臓器にいるMuse細胞はそれぞれの臓器の特徴的な細胞に分化し傷害細胞や死細胞を置き換えることで、ミクロレベルの修復を担っていると考えられております。
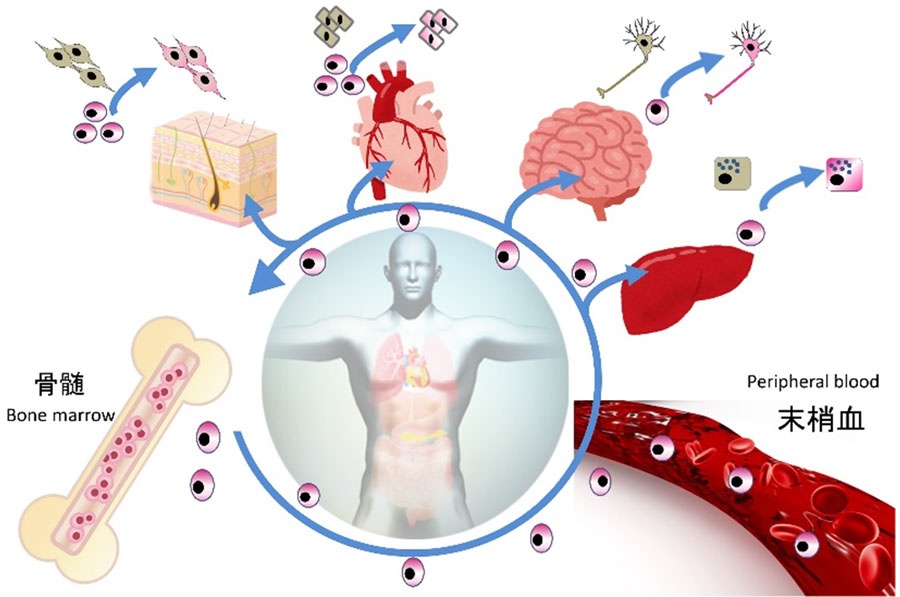
実際に末梢血中へのMuse細胞の動員数が多い患者さんほど、臓器の機能回復が有意であることを示すデーターが臨床の研究から示されています。このことから、Muse細胞が我々の体内で修復幹細胞として機能を担っていることが考えられます。
なぜ点滴だけで様々な臓器が治せるのか
臓器は傷害されると様々な警報シグナルを出します。中でもスフィンゴシン-1-リン酸は、細胞膜の成分であるスフィンゴシンから合成されるため、臓器特異性を超えた普遍的なシグナルです。どの臓器も細胞から作られています。細胞膜の構成成分から転換されるということは、どの臓器であっても傷害を受ければ基本的にはスフィンゴシン-1-リン酸を積極的に産生するということになります。
Muse細胞はスフィンゴシン-1-リン酸に対する受容体を発現しているため、体内を循環中にどこが傷害臓器であるかを検知し、選択的に集積することができます。このような能力は生体にもともと備わっているMuse細胞だけでなく、ドナー由来など体外で調整したMuse細胞であっても同様です。
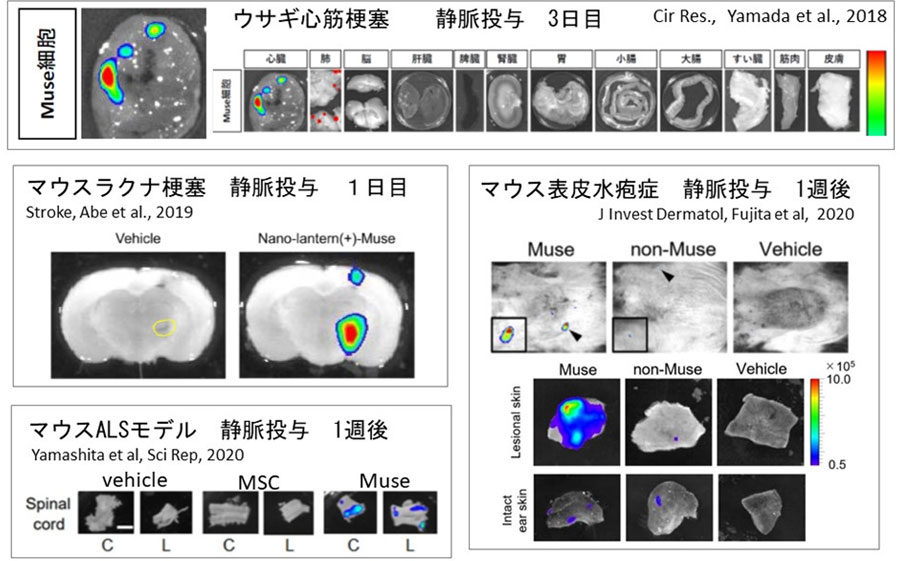
たとえばウサギの心筋梗塞モデルに静脈からMuse細胞を投与したものでは、3日目で心臓の梗塞領域に集積しておりますが、そのほかの健常組織はスフィンゴシン-1-リン酸を出さないため集積が見られません。
マウスの脳梗塞(ラクナ梗塞)では静脈から投与されたMuse細胞は一日で限局した梗塞部位に集積が認められます。
慢性的に進行する筋萎縮性側索硬化症(ALS)や表皮水疱症でも静脈投与されたMuse細胞は神経細胞変性が起きている脊髄の頚髄や腰髄に、また水疱・潰瘍となった部位の皮膚に集積することが見られています。
傷害が広範囲で重篤である場合、あるいは生体にあるMuse細胞が基礎疾患などの理由で活性が損なわれ、十分な修復ができないような場合、外から活性の高いMuse細胞を投与し補充することによって、効果的に臓器の修復をすることが可能であると考えられています。基本的に血管投与で傷害部位に集積しますので、点滴での治療が可能となります。
なぜ外科手術や遺伝子導入、人為的な誘導は必要ではないのか
上述のように、Muse細胞は臓器に共通の警報シグナル、スフィンゴシン-1-リン酸を検知し傷害臓器に選択的に集積するため、目的とする臓器に細胞を届けるための外科手術は基本的に必要ありません。点滴で治療が可能となります。
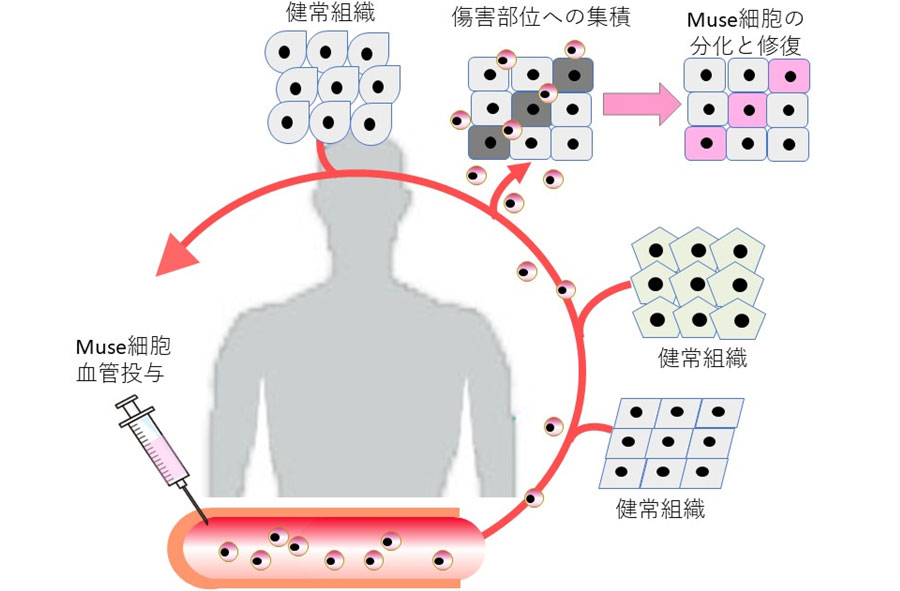
また傷害臓器に集積した後、その臓器に特徴的な機能性の細胞、例えば脳であれば神経細胞とグリア細胞、心臓であれば心筋細胞、腎臓であれば糸球体を構成する足細胞、メサンギウム細胞、肝臓であれば肝細胞や胆管細胞など、それぞれの臓器に応じた細胞に自発的に分化をし、傷害細胞・死細胞を置き換えて組織を修復に導きます。またどの臓器であっても必ず必要となるのが栄養を補給するための血管です。Muse細胞は多能性ですので、血管の細胞にも分化し、血管新生も行います。
このような「場の論理」に応じた分化をするため、遺伝子導入や人為的な誘導操作で目的とする細胞への分化誘導は不要となります。

なぜドナー由来Muse細胞がそのまま投与できるのか
臓器であれ細胞であれ、通常ドナーから提供を受ける場合にはヒト白血球型(HLA)適合検査が求められ、さらに移植後は長期間にわたり免疫抑制剤を必要とされます。しかしMuse細胞ではこのいずれも必要とされません。実際に治験が行われている7つの疾患では、すべてがHLA適合検査や免疫抑制剤投与のいずれもなしに、ドナー由来のMuse細胞製剤がそのまま点滴で投与されております。
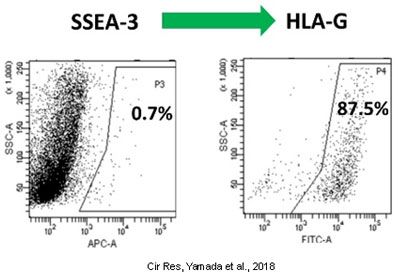
いくつかの動物実験から、ドナー由来のMuse細胞は免疫寛容を引き起こし免疫系の攻撃、すなわち免疫拒絶を受けなくなることが示唆されております。その全容はまだ解明されておりませんが、一つの機構として注目されているのがHLA-Gです。
HLA-Gは胎盤での免疫抑制機構に関与する分子です。胎児は母体にとって非自己であり免疫攻撃の対象となりますが、胎盤ではHLA-Gが発現するため母体の免疫細胞に抑制性のシグナルが入り、胎児は免疫攻撃を免れることが可能となります。
Muse細胞は高率でHLA-Gを発現するため、ドナー細胞が投与されても、同様の機構で免疫攻撃を免れ、傷害組織に到達して「場の論理」に応じた分化を成し遂げ、組織修復をすると考えられています

ウサギはヒト同様に個体間の拒絶の強い動物です。ウサギの心筋梗塞モデルに別個体から採取したMuse細胞を血管から投与しますと、半年にわたりドナー由来Muse細胞は梗塞部位において心筋細胞として生存し続けることが示されております。
その他の有益な作用にはどんなものがあるのか
血管保護作用、臓器の保護効果、細胞死抑制効果、線維化抑制効果などの効果があります。Muse細胞は血管を保護する因子や細胞死を抑制し傷害を軽減する因子、また線維化を抑える因子を産生する能力があり、さらに傷害臓器に長期間にわたり生存するため、これらの効果が持続性を持ちます。
また脳梗塞などの急性の虚血性の疾患や変性疾患だけでなく、重篤な感染症による臓器傷害、たとえば病原性大腸菌O157のベロ毒素による急性脳症のような場合においても、血管投与されたMuse細胞は脳組織に集積し、細胞死に陥った神経細胞を分化によって置換するだけでなく、傷害を受けた神経細胞を保護し脳内血管の破綻を抑制するなど、強い保護効果をもたらすことが報告されています。
Muse細胞が描く新しい医療とは
Muse細胞のメリット、すなわち
- 外科手術が不要で点滴投与で治療が可能
- 遺伝子導入や人為的な分化誘導操作が不要
- ドナー細胞をHLA適合検査や長期の免疫抑制剤投与無しにそのまま使用できる
という特徴を活かせば、身近な治療が可能になることが考えられます。
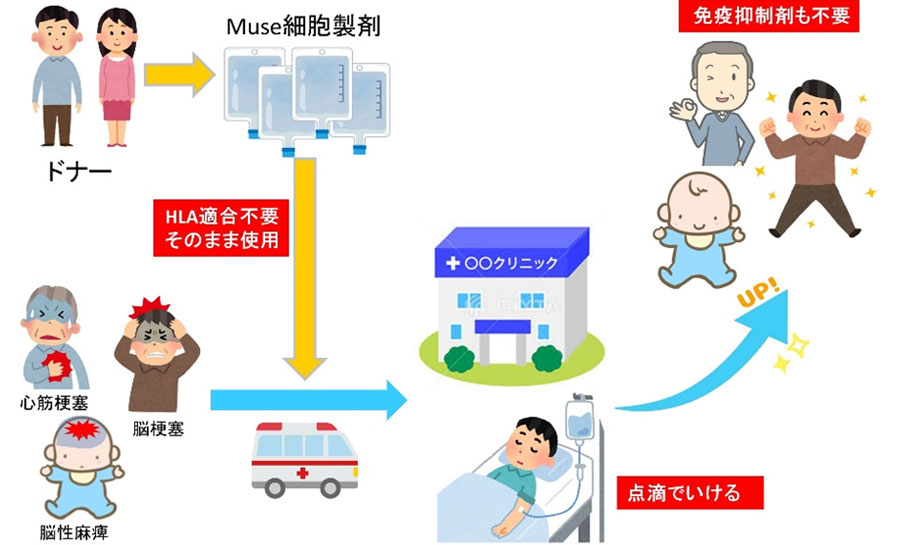
ドナーMuse細胞製剤を保存し準備しておけば、一般病院に運搬し、そのまま点滴で投与できますので、身近な医療機関でもMuse細胞治療が可能となります。臓器移植や骨髄移植などで必要とされる長期の免疫抑制剤投与も必要としないことは、患者さんにとってのメリットとなると思われます。
またこのような流れでの治療が可能であれば、医療格差の是正にも役立つかもしれません。医療アクセスが問題となる地域、たとえば離島や山間部であっても、Muse細胞治療は可能となるかもしれません。
治験と研究開発について
現在まで、心筋梗塞、脳梗塞、表皮水疱症、脊髄損傷、新生児低酸素性虚血性脳症(脳性麻痺)、筋萎縮性側索硬化症(ALS)、急性呼吸逼迫症候群(新型コロナ重症肺炎)に対し、医師主導治験も含めて7つの治験が実施されております。
【脳梗塞治験の概略】
標準的な急性期治療を行った後でも身体機能障害((歩行・トイレ・食事・入浴に常に介助が必要など)を有する脳梗塞発症後 14 日から28 日以内(亜急性期)の患者を対象に行われました。Muse細胞製剤であるCL2020もしくは偽薬をランダムに二重盲検(患者さんにも医師にも、どちらが投与されたか伏せられた状態)の下で行われました。HLA適合検査や免疫抑制剤の投与は行わずにドナー由来のMuse細胞製剤 CL2020(実薬)ないし偽薬が単回投与され、安全性及び有効性についての評価が行われました。
1年後の結果:
【安全性】
- 実薬投与による重大な副作用は認められませんでした。
【有効性】
- 実薬を投与された方では、公共交通機関を利用できるなど介助なしに身の回りのことができる状態まで回復した方が1年後に約7割(22人中15人)に達しましたが、偽薬を投与された方では約38%(8人中3人)でした。
- 実薬を投与された方の約3割(22人中7人)が日常生活には問題がなく、職場復帰を果たせる状態でしたが、偽薬を投与された方で職場復帰を果たせる状態の方はおられませんでした。
偽薬を投与された方と比べて実薬を投与された方では、上肢機能の回復が優れていました。
これらの情報は
https://www.lsii.co.jp/assets/pdf/20210518-1.pdf
で公表されております。
今後のMuse細胞の特性を生かした研究を目指して参りたいと思っておりますが、そのためには研究を推進する費用が必要となります。皆様からのご寄付をいただくことができれば、研究テーマを募り、助成金を出して研究を推進することが可能となります。どうかご協力お願いいたします。
